Klinisch geneticus en universitair hoofddocent Stefan Barakat begon 2,5 jaar geleden met een nieuw project: het DNA van honderd patiënten waarbij een diagnose was uitgebleven in kaart brengen. Dat was mogelijk omdat whole genome sequencing, een techniek om het hele DNA in kaart te brengen, de laatste jaren goedkoper en toegankelijker is geworden.
Bij de eerste twee patiënten was het gelijk raak. Bij twee tienerbroers werd een mutatie gevonden die bij routinediagnostiek over het hoofd gezien was. Ze waren al een aantal jaar patiënt bij het Erasmus MC Sophia Kinderziekenhuis vanwege een –toen nog – onbekend syndroom. Ze hebben moeite met lopen, omdat met name de bovenbeenspier te veel aanspant. Een diagnose bleef uit, totdat Barakat en zijn team dus een mutatie vonden op beide kopieën van het AMFR-gen.
Stamcellen
Wat de functie van het AMFR-gen is, is dan nog onbekend. Barakat: ‘Er was ook vrijwel geen literatuur te vinden, dus we moesten zelf op onderzoek uit.’ Het team neemt stamcellen, fabriceert daar breincellen van en brengt een mutatie aan die het AMFR-gen uitschakelt. Dat zorgde voor een verhoogde opslag van cholesterol in de breincellen.
Als het endoplasmatisch reticulum de kluswinkel is, is dit gen één van de conciërges.
Het AMFR-gen blijkt in te grijpen op het endoplasmatisch reticulum, dat Barakat ook wel de kluswinkel van de cel noemt. ‘Als het endoplasmatisch reticulum de kluswinkel is, is dit gen één van de conciërges. Het reguleert eiwitten die zowel de vetproductie stimuleren als beperken. Als het AMFR-gen niet goed werkt, raakt die verhouding uit balans en krijg je een overschot van cholesterol, met name in zenuwcellen.’

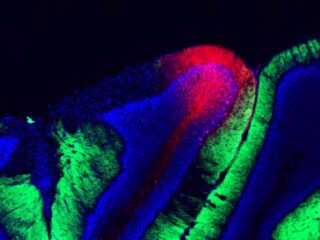
Cholesterol (in rood) hoopt op in een cel. Links een normale cel, rechts met mutatie in het AMFR-gen.
De meeste mensen kennen cholesterol als een vet dat je moet vermijden als je hartproblemen wilt voorkomen. Maar cholesterol is in principe in cellen aanwezig als bouwblok, bijvoorbeeld in het celmembraam: het omhulsel van de cel. Is er te veel van wordt het stijf, is er te weinig dan wordt het slap. ‘Zenuwcellen van soms wel anderhalve meter geven signalen door van je brein naar je benen. Je kan je voorstellen dat als er iets misgaat met de vethuishouding in die cellen dat die signalen niet meer goed doorkomen’, aldus Barakat. Dat verklaart dus mogelijk waarom de broers moeite hadden met lopen.
Zwemcapaciteit
Door naar de volgende stap: de onderzoekers brengen in de larven van zebravisjes dezelfde AMFR-mutatie aan. Dit bevestigt de theorie van Barakat. Deze visjes hebben een soortgelijke motorische stoornis als de patiënten; zwemmen gaat minder goed. De zenuwcellen van de larven blijken veel minder vertakt.
Omdat de onderzoekers weten dat het ligt aan de cholesterolhuishouding, hoeven ze niet lang te zoeken naar een mogelijk medicijn. Bij veel mensen liggen cholesterolverlagers in het medicijnkastje. Barakat: ‘Ik schat dat tien procent van de mensen in Nederland medicijnen slikt om cholesterol te verlagen.’ Wanneer de onderzoekers de larven een standaard cholesterolverlagend medicijn geven tijdens hun ontwikkeling, krijgen de meesten hun zwemcapaciteiten terug en groeien de zenuwcellen weer normaal.
Mensenkinderen
Dus nu, het medicijn voorschrijven aan de broers? Dat kan niet zomaar, want mensenkinderen zijn geen zebravissen en slikken over het algemeen ook geen cholesterolverlagende medicijnen. Er moet eerst bij mensen onderzocht worden of cholesterolverlagende medicijnen echt effectief zijn voor deze aandoening. Wel blijkt uit eerder onderzoek dat het een veilig te gebruiken medicijn is voor kinderen, bijvoorbeeld als die erfelijke vormen van te hoog cholesterol hebben.
Op dit moment kijkt Barakat met collega’s van de kinderneurologie of ze een klinische studie op kunnen zetten. ‘We brainstormen over het gebruiken van het Kinderhersenlab van het Erasmus MC Sophia Kinderziekenhuis. Ze hebben daar een loopband en andere geavanceerde meetapparatuur om alle cognitieve en motorische functies van de tieners volledig in kaart brengen.’

Onderzoeker Eva Medico Salsench bekijkt de zebravissenlarven onder de microscoop.
Zodra het onderzoeksprotocol door de Medisch Ethische Toetsingscommissie is goedgekeurd en de data verzameld zijn, hopen Barakat en zijn collega’s de medicijnen aan te kunnen bieden. ‘Mochten de medicijnen dan aanslaan, kunnen we heel precies de vooruitgang in de gaten houden, om echt te kunnen concluderen of dit bij mensen ook werkt. Het blijft een lange weg, ondanks onze veelbelovende resultaten van de zebravis.’
Tinder
Dat betekent niet alleen voor de Rotterdamse broers een mogelijke behandeling. Op de ‘Tinder voor genetici’ – ofwel de website GeneMatcher – vonden de onderzoekers wereldwijd nog 18 andere patiënten met dezelfde mutatie. De kans is groot dat er wereldwijd nog veel meer patiënten met deze aandoening zijn, die op dit moment nog niet gediagnosticeerd zijn, en die nu pas aan het licht komen door deze studie.
Opluchting
Het mooie van dit onderzoek, gepubliceerd in Acta Neuropathologica, vindt Barakat dat alles samenkomt: ‘De mutatie vinden met nieuwe technologie, de werking van het gen uitpluizen en een mogelijk medicijn opsporen. We zijn iets te weten gekomen over de cholesterolhuishouding in hersencellen en dragen zo bij aan fundamentele kennis over het menselijk lichaam.’
‘Tegelijkertijd is de impact ook duidelijk. Niet alleen voor de patiënten, maar ook voor broers of zussen die misschien drager van de erfelijke aanleg zijn en voor ouders die vaak met een misplaatst schuldgevoel rondlopen. Een diagnose kan al een hele opluchting zijn.’