“Vroeger had ik de wens om sterrenkundige te worden”, vertelt prof. dr. Natasja de Groot. “Dat je uit licht de samenstelling van planeten en sterren kunt bepalen, dat leek me geweldig. Uiteindelijk koos ik voor geneeskunde. Het omgaan met mensen vind ik ook heel leuk.”

Mateloos interessant
Tijdens haar geneeskundestudie wist De Groot al dat ze cardioloog wilde worden, maar dan wel gecombineerd met wetenschappelijk onderzoek. Haar promotieonderzoek (in Leiden en Maastricht) bracht haar in contact met een expert op het gebied van atriumfibrilleren (ook boezemfibrilleren genoemd), een veelvoorkomende hartritmestoornis. “De elektrofysiologie, de wetenschap die zich richt op de diagnostiek en therapie van hartritmestoornissen, was toen een opkomend vak. Ik vond het mateloos interessant.”
Patiëntencontact
In 2009 kwam De Groot bij het Erasmus MC werken. “Ik kon aan de slag als elektrofysioloog én ik kon mijn eigen onderzoeksgroep starten. Research is mijn hoofdtaak, dat vind ik geweldig, maar het contact met patiënten en het uitvoeren van katheterablaties zou ik ook niet willen missen. Ik werk samen met een hoogleraar uit de VUmc en twee hoogleraren van de TU Delft, waarvan er één signalen uit de ruimte analyseert. En een van de postdoc-onderzoekers uit mijn onderzoeksgroep is sterrenkundige.” Lachend: “Een beetje sterrenkunde zit er dus wel in mijn werk.”
Puzzelen
“Waarom ik zo van wetenschappelijk onderzoek houd? Bij mijn promotie kreeg ik van iemand het boek: The pleasure of finding things out. Dat is denk ik wat mij als wetenschapper drijft. Ik vind het heel leuk om dingen uit te puzzelen. Waarom is iets zo?”
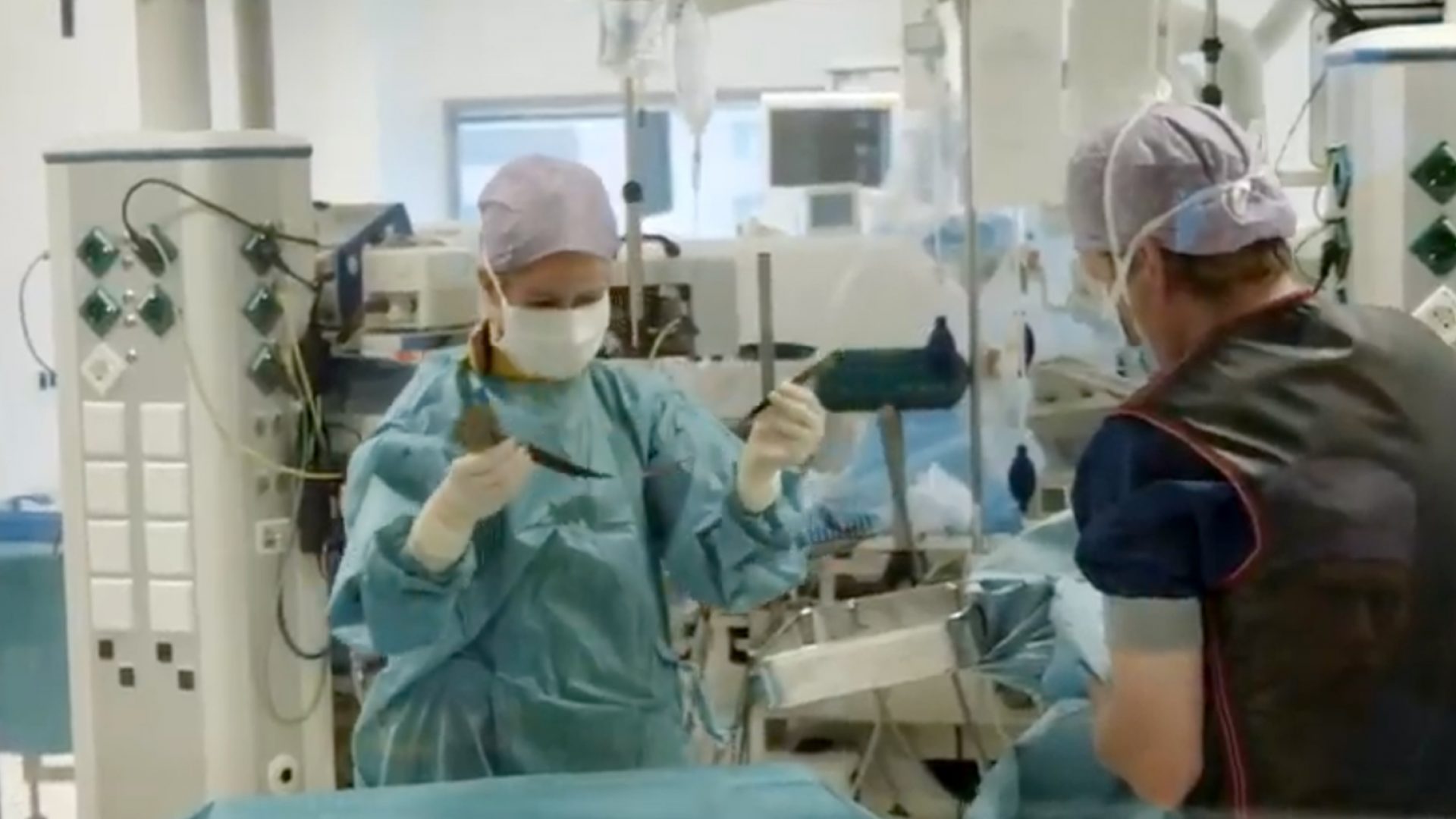
De Groot bestudeert het mechanisme van hartritmestoornissen, van atriumfibrilleren in het bijzonder. Ze legt uit hoe ze aan haar meetgegevens komt: “Tijdens openhartoperaties legt de chirurg een elektrode op het hart, een plaatje met 192 meetpunten. Volgens een vast schema wordt de elektrode over de boezems van het hart geschoven. De boezems zijn holten in het hart die zich boven de hartkamers bevinden. De informatie uit deze metingen zijn zo nauwkeurig, dat kan bijvoorbeeld met metingen aan het lichaamsoppervlak (elektrocardiogram, het ‘hartfilmpje’) nooit worden bereikt. De metingen worden verricht bij patiënten die aan het hart worden geopereerd vanwege een hartklepafwijking, een afwijking aan de kransslagader, of vanwege een aangeboren hartafwijking. Dat zijn zowel mensen mét als zonder hartritmestoornissen. Met die metingen hebben we al baanbrekende inzichten gekregen in signalen en activatiepatronen en we hopen in de komende jaren nog meer te ontdekken.”
Boezem- of atriumfibrilleren
- Bij boezem- of atriumfibrilleren kan de patiënt last hebben van hartkloppingen, een fladderend gevoel op de borst, vermoeidheid, maar sommige patiënten voelen niets bijzonders en hun aandoening wordt bijvoorbeeld bij een sportkeuring ontdekt.
- Atriumfibrilleren is de meest voorkomende hartritmestoornis.
- In de Europese Unie lijden 7 miljoen mensen aan deze aandoening.
- In Nederland zijn meer dan 200.000 patiënten met atriumfibrilleren. Het wordt dan ook de cardiovasculaire-epidemie genoemd.
- Ondanks alle technologische innovaties op het gebied van onder andere mapping en ablatie-technieken, kan de ritmestoornis bij de meeste patiënten nog steeds niet verholpen worden.

Wat doet een elektrofysioloog?
Een elektrofysioloog voert invasieve therapieën uit: tijdens de behandeling worden instrumenten in het lichaam gebracht. Denk aan het plaatsen van een pacemaker (een apparaatje dat bij een vertraagd hartritme het hart met een elektrisch stroomstootje weer op gang helpt) of ICD (een pacemaker die bovendien elektrische shocks afgeeft als het hart levensbedreigende hartritmestoornissen heeft), of het verrichten van een katheterablatie. Daarbij worden met een katheter met behulp van elektrische energie op gecontroleerde wijze littekenweefsel in de hartspier veroorzaakt, waardoor de ritmestoornis verdwijnt.
Je wordt elektrofysioloog na een langdurig opleidingstraject: na een studie geneeskunde en de opleiding tot cardioloog volgt een tweede specialisatie tot elektrofysioloog.

Blokjespatroon
De Groot toont een video met gekleurde blokjes. “Wanneer een elektrische golf het meetpunt in de electrode passeert ontstaat een signaal. De snelheid waarmee dat gebeurt kun je uitdrukken in een kleur. De snelste golf krijgt een rode kleur, de daaropvolgende blauw, enzovoort. Zo kun je ritmestoornissen visualiseren. Normaal gesproken verplaatst het elektrisch signaal zich geordend over de hartspier en ziet het blokjespatroon er regelmatig uit. Bij patiënten met een hartritmestoornissen is dat verloop een stuk grilliger, de elektrische golven verplaatsen zich asynchroon en in drie dimensies door het hart. Wij hebben als eerste ter wereld laten zien dat de binnen- en buitenlaag van het hart elektrisch los van elkaar liggen bij patiënten met boezemfibrilleren.”
Vergelijken
De Groot: “De meeste mensen worden geboren met een hart dat de elektrische signalen netjes geleidt. Naarmate je ouder wordt, treden er verstoringen op in die geleiding. Dat kan komen door de veroudering zelf, maar ook door een longafwijking, hoge bloeddruk of suikerziekte. Ook overgewicht, roken en het drinken van alcohol kunnen van invloed zijn. Dat schadeproces wordt elektropathologie genoemd. Bij een bepaalde mate van elektropathologie is de kans groot dat je een hartritmestoornis ontwikkelt. Althans, dat is onze hypothese.”
Neerwaartse spiraal
“We zijn de geleidingseigenschappen en signaaleigenschappen gaan kwantificeren. We drukken de ernst van de stoornis uit in getallen. Door de metingen te analyseren hopen we antwoord te vinden op een paar belangrijke vragen: waar bestaat die elektropathologie uit? En welke elektropathologie is specifiek voor patiënten met boezemfibrilleren? Boezemfibrilleren komt voor in een aanvalsgewijze vorm die over kan gaan in een permanente vorm. Hoe dat komt? Boezemfibrilleren wordt veroorzaakt door schade aan het hart, maar boezemfibrilleren beschadigt de hartspier zelf ook. Je belandt in een neerwaartse spiraal: de fibrillatie-episodes gaan steeds langer duren, totdat ze niet meer vanzelf stoppen.”
Risico
“Omdat we onze metingen omzetten in getallen, kunnen we patiënten met elkaar vergelijken. We krijgen profielen die tonen of iemand een hoog of een laag risico loopt op het krijgen van een hartritmestoornis. Bij 30% van de patiënten die aan hun hart geopereerd worden, treedt in de eerste drie dagen na de operatie atriumfibrilleren op. Hoe dat komt weten we niet. We proberen met onze metingen vast te stellen of we het stadium van de ritmestoornis kunnen bepalen en of we kunnen voorspellen welke patiënten atriumfibrilleren gaan ontwikkelen en welke niet.”
Alternatief
“Atriumfibrilleren is moeilijk te behandelen. Ablatie is, ondanks alle recente nieuwe mapping en ablatie technieken maar bij 50% van de patiënten effectief. Dat is voor zo’n kostbare en ingrijpende behandeling natuurlijk veel te laag. We moeten een diagnostischetoolhebben, een hulpmiddel waarmee we van tevoren kunnen bepalen welke patiënt gebaat is met een ablatie en welke niet. Je kunt hartritmestoornissen niet op een hoop gooien, ze hebben verschillende oorzaken en vragen dus ook om verschillende behandelingen.”

Elektrodevest
Nu worden de metingen nog verricht met behulp van een relatief zware ingreep: de elektrode wordt tijdens een operatie op het hart geplaatst. De Groot en haar collega’s onderzoeken of de metingen eenvoudiger kunnen plaatsvinden. “Bijvoorbeeld met een katheter. Maar het zou nog mooier zijn als we onze metingen zouden kunnen verrichten met behulp van een non-invasieve methode, bijvoorbeeld met meerdere elektrodes aan de buitenkant van het lichaam, zoals een elektrodevest. Echter zijn de huidige beschikbare, commercieel verkrijgbare technieken bij lange na niet nauwkeurig genoeg. Je kunt immers elektrische golven van 1 millimeterbreedniet zien aan het lichaamsoppervlak, dat is technisch onmogelijk.”
Biomarkers
De Groot werkt binnen het AFFIP (Atrial Fibrillation FIngerPrinting)-consortium samen met bioloog prof. dr. Bianca Brundel (Amsterdam UMC) en twee hoogleraren van TU Delft: Wouter Serdijn, een micro-elektronica-expert, en Alle-Jan van der Veen, een deskundige op het gebied van signaalanalyse. “We kijken naar de elektrische afwijkingen en de veranderingen op het niveau van de hartspiercel. En we speuren naar biomarkers: komen in het bloed stofjes voor waaraan je kunt zien dat er iets mis gaat met de elektrische signalen in het hart? Als we die vinden, is dat mogelijk ook een manier om af te komen van onze invasieve meetmethode.”

Meedoen
Veel patiënten willen aan het onderzoek meedoen. De Groot: “Wat we van hen vragen is niet gering. Bij patiënten die niet aan boezemfibrilleren lijden, meten we eerst de normale situatie van het hart, daarna wekken we boezemfibrilleren op om te zien hoe de elektrische signalen zich door de hartspier verplaatsen. Op zich is die ingreep niet gevaarlijk, maar het idee dat een hartritmestoornis wordt opgewekt is niet niks. Desondanks zijn veel patiënten bereid om aan de studie mee te werken. Daar ben ik heel blij mee.”
Meer over het werk van prof. dr. Natasja de Groot leest u hier.